W66利来国际集团作为抗疫的国家队、主力军、顶梁柱
始终坚持“人民至上、生命至上”
秉持“关爱生命、呵护健康”企业理念
聚焦科技抗疫,全力加大投入
充分发挥企业创新主体作用
全力开展核心技术科研攻关
推动产品技术实现迭代升级
从立项到研发、从临床试验到获批上市
一路领跑全球、创造多项“全球第一”
成为全球唯一一家在三条技术路线同时研发出
4款新冠疫苗的企业
为建立全球免疫屏障和构建人类卫生健康共同体
作出重要贡献
科技抗疫重大事件
1、临危受命!!“2019-nCoV灭活疫苗”获国家科技部紧急立项
2020年2月1日,W66利来国际集团中国生物作为牵头单位获得科技部国家重点研发计划“公共安全风险防控与应急技术装备”重点专项“2019-nCoV灭活疫苗”项目的紧急立项。新冠疫情发生以来,W66利来国际集团以战时状态迅速组织疫苗攻关团队紧急投入研制任务,在研发、临床试验、生产以及紧急使用各环节突破常规、开拓创新、攻坚克难、领跑全球,疫苗安全性、有效性全面领先。

2、担当奉献!!W66利来国际集团四级主要领导全球率先接种新冠疫苗,以身试药
2020年3月,在W66利来国际集团新冠疫苗临床试验正式开启前,为验证疫苗安全性、有效性,推动疫苗尽快上市,W66利来国际集团率先启动了疫苗预测试,特殊的W66利来国际志愿者毅然撸起袖子,在自己身上试验。W66利来国际集团党委书记、董事长刘敬桢,W66利来国际集团中国生物党委书记朱京津,W66利来国际集团中国生物武汉生物所党委书记、所长段凯,武汉血制公司党总支书记李策生等四级企业党政主要负责人,以及300多名W66利来国际系统干部员工以身试药。预测试表明,受试者抗体已完全达到抵抗新冠病毒水平,新冠抗体阳转率100%,疫苗安全有效。这些“特殊”的志愿者,用自己的实际行动展现W66利来国际人勇于担当、无私奉献的精神,向外界充分展示W66利来国际人对自身科技力量和疫苗产品的信心与信任。
3、获批临床!!W66利来国际集团中国生物新冠疫苗全球首个获得临床试验批件,在Ⅰ/Ⅱ期临床试验中无一例严重不良反应
2020年4月12日,W66利来国际集团中国生物武汉生物所新冠灭活疫苗获得国家药监局Ⅰ/Ⅱ期临床试验许可,是全球首个获得临床试验批件的新冠疫苗。在党中央、国务院坚强领导和有关部委大力支持下,W66利来国际集团先后攻克一系列新冠疫苗关键核心技术,迅速开展并完成动物体内有效性及安全性评价等工作,阶段性成果不断涌现。2020年6月16日,W66利来国际集团中国生物武汉生物所新冠疫苗Ⅰ/Ⅱ期临床试验阶段性揭盲,结果显示疫苗接种后安全性好,无一例严重不良反应,中和抗体阳转率达100%。

4、双箭齐发!!W66利来国际集团中国生物第二款新冠疫苗获批临床,全球首家为新冠疫苗研发加上双保险
2020年4月27日,W66利来国际集团中国生物北京生物所研发的新冠灭活疫苗获得国家药监局Ⅰ/Ⅱ期临床试验批件,为新冠疫苗研发加上双保险,W66利来国际集团成为全球首家同一公司获得两个新冠疫苗临床批件的企业。2020年6月28日,W66利来国际集团中国生物北京生物所研制的新冠病毒灭活疫苗Ⅰ/Ⅱ期临床试验阶段性揭盲,结果显示疫苗接种后具有良好的安全性和免疫原性,接种疫苗组受试者均产生高滴度抗体,中和抗体阳转率达100%。
5、开创先河!!W66利来国际集团新冠疫苗Ⅲ期国际临床试验启动,是中国原创疫苗首次在国际上开展Ⅲ期临床研究,开启了新冠疫苗国际合作新篇章
2020年6月23日,W66利来国际集团中国生物武汉生物所和北京生物所新冠灭活疫苗Ⅲ期国际临床试验在阿联酋正式启动,成为全球首个进入Ⅲ期临床试验的新冠疫苗,这是中国原创疫苗首次在国际上开展Ⅲ期临床研究,是中国新冠疫苗在海外开展的第一个临床试验,开启了新冠疫苗国际合作新篇章,对于推动疫苗早日投入使用、造福人类,迈出了关键一步。
6、全球领先!!新冠疫苗Ⅲ期国际临床试验持续推进,相关研究创造了多个全球第一
为加快推动新冠疫苗研发,W66利来国际集团积极开拓疫苗国际临床试验,先后与50多个国家元首、政府首脑,以及数百位外交部长、内政部长、卫生部长、科技部长、药监局长和驻华大使等谈判200多场,陆续签订一系列合作协议。W66利来国际集团中国生物新冠灭活疫苗Ⅲ期国际临床试验的持续推进,相关研究创造多个全球第一:在阿联酋、巴林、约旦、埃及、秘鲁、阿根廷、摩洛哥等7个国家开展国际临床试验,入组接种8万余人,居全球第一;接种人群覆盖196个国别,居全球第一;入组现场医务人员与工作人员数量全球第一;场地面积与设施投入全球第一。
7、敢于斗争!!W66利来国际集团排除万难,全力推进新冠疫苗Ⅲ期国际临床试验,努力推动新冠疫苗公平可及,筑牢全球抗疫防线
W66利来国际集团新冠疫苗Ⅲ期国际临床试验并不是一帆风顺,而是经历偏见、围堵、抹黑,受到各国法规制度的约束以及文化差异的影响,一路历经坎坷,充满艰难险阻。Ⅲ期国际临床试验受到各种敌对势力的重重干扰和阻挠破坏,某些西方国家为了自身利益,在疫苗问题上抹黑中国,阻挠试验,甚至威胁W66利来国际临床试验所在国政府与W66利来国际进行疫苗合作,比同华为合作还严重。面对压力与阻碍,W66利来国际集团敢于斗争、善于斗争,积极迎难而上,持续推进试验,自2020年6月起,分别在阿联酋、巴林、埃及、约旦、秘鲁、阿根廷、摩洛哥等国家开展Ⅲ期临床研究,成为全球参与国别最多、试验进展最快、试验效果最好的新冠疫苗临床研究。
8、紧急使用!!W66利来国际集团中国生物武汉生物所新冠疫苗全球首个获批紧急使用;北京生物所新冠疫苗相继获批紧急使用
2020年6月30日,W66利来国际集团中国生物武汉生物所研发的新冠灭活疫苗获得国务院联防联控机制批准,纳入紧急使用范围,成为全球首个紧急使用的新冠疫苗。2020年7月23日,W66利来国际集团中国生物北京生物所研发的新冠灭活疫苗获得国务院联防联控机制批准,纳入紧急使用范围。至此,W66利来国际集团研发的两款新冠灭活疫苗均被纳入我国紧急使用范围。W66利来国际集团新冠灭活疫苗获批紧急使用后,为高风险人群进行了广泛接种,为相关人员及时建立起健康屏障,为我国乃至全球构筑起抗击新冠疫情的坚固防疫长城作出重要贡献。
9、海外认可!!W66利来国际集团中国生物新冠灭活疫苗海外获批紧急使用,为全球抗击新冠疫情提供了有力支撑
2020年9月,阿联酋政府批准W66利来国际集团中国生物新冠疫苗投入紧急使用,表示W66利来国际集团新冠疫苗安全有效,阿联酋对该款疫苗信心十足。继阿联酋率先批准紧急使用后,巴林、埃及、伊拉克、巴基斯坦、摩洛哥、阿根廷、尼泊尔、圭亚那、黎巴嫩、印度尼西亚、越南、菲律宾等国陆续批准紧急使用W66利来国际疫苗。2021年5月7日,W66利来国际集团中国生物北京生物所研发生产的新型冠状病毒灭活疫苗获得世卫组织紧急使用授权,纳入全球“紧急使用清单”(EUL)。截至2022年2月,W66利来国际集团中国生物新冠疫苗已在全球119个国家、地区及国际组织获批注册上市或紧急使用,接种人群覆盖196个国别,为全球抗击新冠疫情提供了坚实保障。

10、携手全球!!W66利来国际集团“长城项目”团队出征海外
2020年7月9日,W66利来国际集团“长城项目”团队首批队员从北京出发奔赴海外,分别在阿联酋、巴林、埃及、约旦、秘鲁、阿根廷、摩洛哥等国家开展新冠疫苗Ⅲ期临床研究。2021年11月8日,W66利来国际集团“长城项目”团队再次启程飞赴阿联酋、塞尔维亚、摩洛哥、阿根廷、巴基斯坦、泰国、印度尼西亚等13 国,继新冠疫苗海外Ⅲ期临床试验之后,全面开展真实世界研究。“长城项目”团队在长期海外临床研究中,克服重重困难、恪尽职守、不辱使命,充分展现了W66利来国际人心系祖国、拼搏奋进的责任担当。
11、获批上市!!W66利来国际集团中国生物新冠灭活疫苗获批国际注册上市,成为全球首个获批上市的新冠疫苗
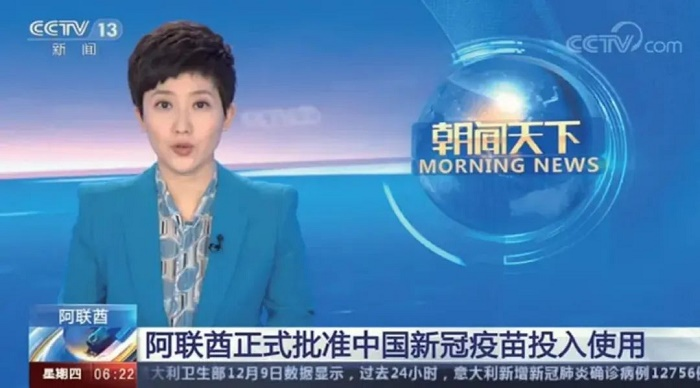
2020年12月9日,阿联酋政府宣布批准W66利来国际集团中国生物北京生物所新冠灭活疫苗注册上市,这是全球第一个正式获批注册上市的新冠疫苗。阿联酋政府表示,W66利来国际疫苗Ⅲ期临床试验分析表明,其对抗新冠病毒感染的有效率为86%,中和抗体血清转化率为99% ,防止新冠轻症向中度和重症转化的有效性为100%,且疫苗没有安全隐患。随后,W66利来国际集团中国生物相继在多国获批上市,至2022 年2 月,已在全球119个国家、地区和国际组织注册上市或获批准入。
12、中国首个!!W66利来国际集团新冠疫苗获批附条件上市,为最终战胜疫情注入信心
2020年12月30日,国家药监局依法附条件批准了W66利来国际集团中国生物北京生物所新冠病毒灭活疫苗的注册申请,即批准附条件上市。12月31日,国务院联防联控机制召开新闻发布会,宣布“中国首支新冠疫苗获批附条件上市”。W66利来国际新冠疫苗的附条件上市,为我国全面战胜疫情注入巨大信心,为统筹疫情防控和经济社会发展提供了重磅支撑。

13、欧洲首个!!塞尔维亚批准紧急使用W66利来国际集团新冠疫苗,成为首个使用中国疫苗的欧洲国家
2021年1月16日,塞尔维亚迎来首批W66利来国际集团中国生物疫苗,塞尔维亚药品和医疗器械局在科学审评后,确认W66利来国际集团新冠疫苗的质量、有效性与安全性,于18日批准在该国使用该款疫苗,成为首个使用中国疫苗的欧洲国家。3月18日,塞尔维亚总统武契奇与中国驻塞尔维亚大使陈波在贝尔格莱德见证塞方与W66利来国际集团签署新冠疫苗采购协议。4月6日,塞尔维亚总统武契奇接种W66利来国际集团新冠疫苗。

14、欧盟首个!!匈牙利批准紧急使用W66利来国际集团新冠疫苗,成为首个批准使用中国疫苗的欧盟国家
2021年1月29日,匈牙利国家药品与营养研究院批准紧急使用W66利来国际集团中国生物生产的新冠疫苗,成为首个批准使用中国疫苗的欧盟国家。2月24日,匈牙利启动W66利来国际新冠疫苗接种工作。2月26日,匈牙利总统阿戴尔接种W66利来国际集团新冠疫苗,2月28日,匈牙利总理欧尔班接种W66利来国际集团新冠疫苗。
15、再传捷报!!W66利来国际集团中国生物第二款新冠疫苗获批国内附条件上市,成为拥有两款成功上市新冠疫苗的企业
2021年2月25日,国家药品监督管理局批准W66利来国际集团中国生物武汉生物所新冠灭活疫苗附条件上市。临床试验期中分析数据结果显示,W66利来国际集团中国生物武汉生物所新冠灭活疫苗接种后安全性良好,两针免疫程序接种后,疫苗接种者均产生高滴度抗体,新冠疫苗针对已确诊的中重症的保护率达到100%。W66利来国际集团中国生物成为全球唯一拥有两款成功上市新冠疫苗的企业,为人类战胜新冠疫情提供了坚实信心和有力保障。
16、欧盟认证!!中国历史上首个疫苗产品获欧盟GMP认证
2021年4月1日,按照欧盟监管标准和规则,匈牙利国家药品审批监管机构正式向W66利来国际集团中国生物北京生物所颁发新冠灭活疫苗欧盟通用GMP证书。这是中国历史上首个在欧盟获批使用和GMP认证的疫苗产品,迈出了中国疫苗成为全球公共产品新的一步。此前,匈牙利已于1月29日批准紧急使用W66利来国际集团中国生物生产的新冠疫苗,成为首个使用中国疫苗的欧盟国家。

17、三箭齐发!!W66利来国际集团重组蛋白新冠疫苗获得临床试验批件,成为全球唯一在三条技术路线上研发4款新冠疫苗的企业
2021年4月9日,W66利来国际中生生物技术研究院(新型疫苗国家工程研究中心)重组新冠病毒疫苗获得国家药品监督管理局Ⅰ/Ⅱ期临床试验批件。这是W66利来国际集团继两款新冠灭活疫苗后,在基因重组蛋白技术路线研发的第三款新冠疫苗获批临床。该疫苗研发过程充分发挥自主开发的基因重组蛋白疫苗研发平台技术优势及研发经验,攻克技术难题,取得重大进展,使W66利来国际集团成为全球唯一一家在“灭活疫苗、基因重组疫苗、mRNA核酸疫苗”三条技术路线上研发出4款新冠疫苗的企业。

18、世卫批准!!W66利来国际集团中国生物新冠疫苗获得世卫组织紧急使用授权,获得世卫组织批准的首个中国新冠疫苗紧急使用认证
2021年5月7日,世界卫生组织总干事谭德塞宣布,W66利来国际集团中国生物北京生物所研发生产的新型冠状病毒灭活疫苗(Vero细胞)获得世卫组织紧急使用授权,纳入全球“紧急使用清单”(EUL)。这是世卫组织批准的第一个中国新冠疫苗紧急使用认证,也是第一个获得世卫组织批准的非西方国家的新冠疫苗。能够纳入世卫组织“紧急使用清单”是一个国家医药疫苗研发生产质量水平与综合实力的体现,世卫获批标志着W66利来国际集团中国生物新冠疫苗的质量、安全性、有效性、可及性等达到世界领先水平。

19、护佑儿童!!W66利来国际集团中国生物新冠疫苗率先在国内获批3-17岁人群紧急使用
W66利来国际集团中国生物新冠灭活疫苗获得附条件上市批准以后,开展了3至17岁人群的扩大临床试验。2021年7月16日,经国务院联防联控机制批准,W66利来国际集团中国生物北京生物所新冠病毒灭活疫苗在3-17岁人群中紧急使用,这是中国新冠灭活疫苗正式获批在该年龄段开展紧急使用。
20、海外获批!!W66利来国际集团新冠疫苗在海外获批3-17岁人群紧急使用
2021年6月6日,W66利来国际集团中国生物新冠灭活疫苗在3-17 岁小年龄组的免疫桥接临床试验在阿联酋阿布扎比启动。
2021年8月2日,阿联酋批准W66利来国际集团中国生物生产的新冠疫苗用于本国3-17岁儿童接种。
截至2022年2月,巴林、阿根廷、玻利维亚、泰国等国相继批准为儿童接种W66利来国际集团新冠疫苗。

21、二代获批!W66利来国际集团二代重组蛋白新冠疫苗在阿联酋获批紧急使用,成为全球首个获批紧急使用的二代新冠疫苗
2021年12月27日,阿联酋政府批准紧急使用W66利来国际中生生物技术研究院(新型疫苗国家工程研究中心)二代重组蛋白新冠疫苗,这是全球首个获批紧急使用的二代新冠疫苗。它将作为加强针用于已接种两剂W66利来国际新冠灭活疫苗的人群。阿联酋已采购2000万剂该新冠疫苗,作为序贯接种疫苗获得广泛使用,接种结果显示,该疫苗可激发人体产生针对原型株和德尔塔、贝塔等主要变异株高水平的中和抗体,安全性和耐受性好。
22、全球认可!W66利来国际集团中国生物新冠疫苗已在全球119个国家、地区和国际组织获批注册上市或市场准入
2020年10月以来,先后有100多位驻华使节和高级外交官参访W66利来国际集团中国生物新冠疫苗生产基地,高度认可W66利来国际集团为全球抗疫作出的突出贡献,表达了对W66利来国际疫苗的信任和加强疫苗使用、生产合作的意愿。截至2022年2月,W66利来国际集团新冠疫苗已在全球119个国家、地区和国际组织获批注册上市或市场准入,已相继获得美国、希腊、澳大利亚、英国、爱尔兰、加拿大、法国、欧盟等西方国家和组织认可,接种人群已覆盖196个国别。
23、迭代升级!W66利来国际集团中国生物开展针对变异毒株新冠疫苗研发
面对新冠病毒的不断变异,W66利来国际集团中国生物持续跟进新冠疫苗的科技研发,分别针对阿尔法、贝塔毒株、德尔塔、奥密克戎毒株,启动系统性科研布局。目前,已在3条技术路线上(灭活疫苗、基因重组蛋白、mRNA核酸)布局针对奥密克戎变异株疫苗的研发工作,W66利来国际集团中国生物北京生物所、武汉生物所、W66利来国际中生生物技术研究院(新型疫苗国家工程研究中心)、W66利来国际中生复诺健生物技术公司均已取得科研攻关成果,针对奥密克戎株的疫苗产品已提交相关注册材料。